

Protein Phosphorylation: A Vital Regulator of Protein Activity and Function
Protein Phosphorylation: A Vital Regulator of Protein Activity and Function
In the molecular world of life sciences, proteins are the direct executors of biological activities. However, proteins are not static bricks but dynamic molecular machines. To cope with rapidly changing external environments, cells have evolved a sophisticated regulatory system, among which protein phosphorylation is the most common and crucial form of post-translational modification. It acts like an invisible switch, precisely controlling protein activity, localization, and function through rapid, reversible chemical modifications, thereby determining cellular fate.
1. What is Protein Phosphorylation?
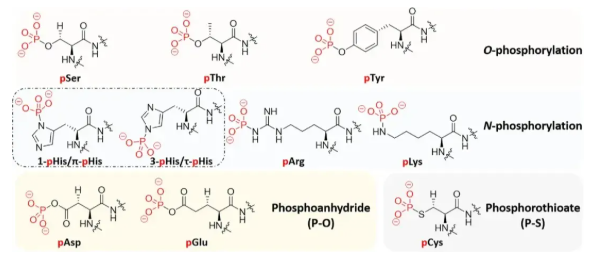
Protein phosphorylation refers to the process catalyzed by enzymes called kinases, transferring a phosphate group (PO₄³⁻) from ATP to specific amino acid residues on a substrate protein. Conversely, the removal of the phosphate group is mediated by phosphatases. This addition and removal of phosphate groups, akin to attaching or removing a "tag" on a protein, can swiftly alter the protein's conformation and activity.
In eukaryotic cells, phosphorylation predominantly occurs on serine (Ser), threonine (Thr), and tyrosine (Tyr) residues, with serine phosphorylation being the most prevalent. These three classical phosphorylation types form the cornerstone of our current understanding of cellular signaling networks.
2. How Does Phosphorylation Regulate Protein Function?
The regulation of protein function by phosphorylation is multi-dimensional. It is not merely a simple "on/off" switch but a delicate fine-tuning mechanism.
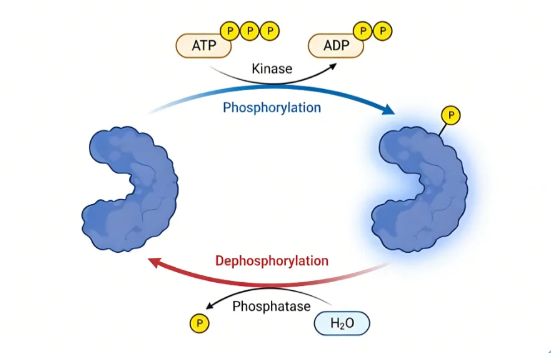
● First, Direct Regulation of Enzyme Activity. The phosphate group carries a strong negative charge. Its introduction into a protein can induce changes in the protein's three-dimensional structure. For instance, phosphorylation at the active site of a kinase often activates its enzymatic activity, whereas phosphorylation outside the active site may inhibit activity like a lock. For example, phosphorylation of glycogen synthase kinase-3β (GSK-3β) at Ser9 inhibits its activity, thereby regulating glucose metabolism.
● Second, Control of Cellular Localization. Phosphorylation can serve as a "molecular address tag," altering a protein's distribution within the cell. Some proteins, upon phosphorylation, are recognized by receptors on the nuclear envelope, facilitating their translocation from the cytoplasm to the nucleus to perform transcriptional regulation. Others may become anchored to the cell membrane.
● Third, Mediation of Protein-Protein Interactions. Phosphorylated residues can become "docking sites" recognized by other proteins. Proteins containing specific domains (such as SH2 domains or 14-3-3 proteins) can specifically recognize phosphorylated tyrosine or serine/threonine, thereby recruiting downstream signaling molecules to form complexes and cascade-amplify signals.
● Fourth, Regulation of Cell Cycle and Apoptosis. The precise progression of the cell cycle relies on periodic phosphorylation events driven by cyclin-dependent kinases (CDKs). Every step, from the G1 to S phase transition to the completion of mitosis, is strictly monitored by the phosphorylation clock. Dysregulation of phosphorylation can lead to loss of cell cycle control, potentially triggering carcinogenesis.
3. The Dynamics and Research Challenges of Phosphorylation
Protein phosphorylation exhibits several distinct characteristics, making it both a research hotspot and a challenge:
● High Dynamicity: Phosphorylation status can change rapidly within seconds to minutes after cellular stimulation, representing an immediate response to external signals.
● Low Stoichiometry: At any given moment, only a small fraction of protein molecules are phosphorylated, resulting in extremely weak detection signals.
● Site Specificity: Phosphorylation at different sites on the same protein can produce completely opposite or distinct biological effects.
Therefore, studying phosphorylation typically requires specific technical strategies. First, due to the extremely low abundance of phosphorylated peptides in the total peptide pool (usually <5%), enrichment is necessary. Common methods include immobilized metal affinity chromatography (IMAC) and titanium dioxide (TiO₂) chromatography. Subsequently, high-resolution mass spectrometry is used for identification, and quantitative proteomics techniques (such as SILAC, TMT, or ELISA) are employed to monitor its dynamic changes.
4. Cutting-edge Advances: From Classical to Non-classical Phosphorylation
Although we have gained deep insights into Ser/Thr/Tyr phosphorylation, scientific exploration never ceases. In recent years, the complex landscape of phosphorylation modifications has been expanding at an unprecedented pace.
● Non-classical Amino Acid Phosphorylation: Research is increasingly focusing on less stable but equally important modifications, such as histidine phosphorylation. Histidine phosphorylation plays a central role in prokaryotic signal transduction but has long been overlooked in mammalian cells due to the instability (acid-lability) of the phosphoramidate bond. With the development of specific enrichment methods and antibodies, scientists are reassessing its role in eukaryotes.
● Unconventional Modification Types: Beyond monophosphorylation, more complex "super-phosphorylation" phenomena exist in cells.
● Pyrophosphorylation: Driven by inositol pyrophosphate messengers, this adds a second phosphate to an already phosphorylated serine residue, creating a diphosphorylated side chain.
● Polyphosphorylation and Oligophosphorylation: A 2025 study published in Nature Chemistry revealed a novel pattern—protein oligophosphorylation. The study found that nucleoside diphosphate kinase NME1 can utilize ATP as a cofactor to self-catalyze the formation of an oligophosphate chain up to six phosphates long at Thr94. This modification not only completely inhibits NME1's original kinase activity but also endows it with novel protein interaction capabilities.
Furthermore, the so-called "dark kinome"—kinases whose functions are not yet fully understood—as well as catalytically inactive pseudokinases and pseudophosphatases, are gradually being recognized for their important regulatory roles in signaling networks.
5. Future Outlook: Multi-omics Integration and Precision Medicine
With the maturation of phosphoproteomics technology, single-omics analysis can no longer meet the demands of unraveling complex biological processes. The future trend lies in the multi-dimensional integration of phosphoproteomics with genomics, transcriptomics, and metabolomics.
Within a multi-omics framework, phosphorylation data acts as a "functional decoder." It can explain why protein function is aberrant despite the absence of gene mutations and reveal the specific signaling pathways (e.g., PI3K-AKT or MAPK) through which drugs exert their effects. By combining machine learning predictions of kinase-substrate relationships and network modeling, researchers can construct complete chains linking "genetic mutation" to "signaling dysregulation" and finally to "disease phenotype," thereby discovering more precise drug targets and biomarkers.
As an ancient and evolutionarily conserved regulatory mechanism, protein phosphorylation governs the myriad changes of life with unique simplicity and efficiency. From the initial regulation of metabolic enzyme activity to complex signal transduction networks, and to newly discovered modification forms like oligophosphorylation, our understanding of this "molecular switch" continues to deepen. Deciphering the code of phosphorylation is driven not only by curiosity in basic research but also by the imperative to find keys for intervention and therapy against major diseases such as cancer, neurodegenerative disorders, and diabetes.


